房颤消融:“冷-热-光-电”的交相辉映
来源:医休器械平台旗下公众号-医休RDN
作者:医休哥
导管消融在心房颤动(简称房颤)中的治疗地位逐渐提高,随着科学技术的进步,消融能量从射频能量的一支独放,逐渐发展为冷冻、激光、脉场波等等多种能量竞相登场;导管的形态从大头导管演变成为球型;导管消融从肺静脉隔离,逐渐应用到肺静脉外的病灶。上述的改变,极大地提高了导管消融的有效性及安全性,拓展了房颤治疗的策略,彻底改变了房颤的预后。
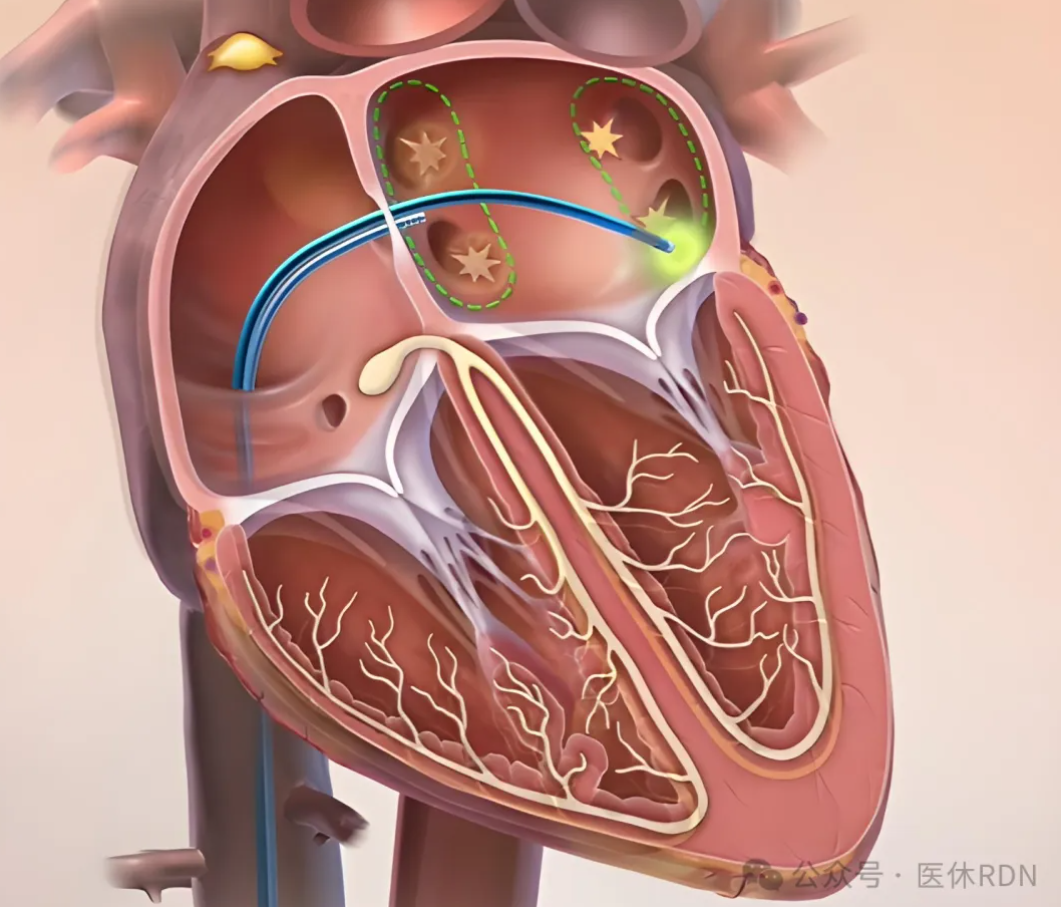
“热”-射频能量
射频能量是目前心律失常消融最为广泛使用的能源之一,于20世纪80年代被应用于临床中。导管形态通常为大头导管,其头端热量通过阻抗热及传导热对心肌组织产生损伤,从而实现安全且有效的消融目的。
在早期的导管研发过程中引入了冷盐水灌注系统与压力感知系统,极大程度减少了血栓形成概率,使导管与组织间贴靠实现量化显示。
对于成功的射频消融来说,精准和稳定的导管操作至关重要。
相较于刚性的手动操作,磁导航系统的引入为导管操作带来更多便利。术者可将柔性射频导管置入心腔后,通过配套计算机控制预设磁场将导管引导至靶点,对于到达复杂靶点方面具有优势,且柔性导管不易引起心脏穿孔。同时术者可在控制室内操作计算机完成消融治疗,极大程度减少术者对射线的暴露。在与手动操作射频消融导管的对比中,磁导航房颤消融的成功率与手动消融相当,而术中发生心包压塞的概率更低;与此同时,磁导航消融的学习曲线更低,操作更易上手。未来磁导航系统与人工智能、5G通信等相关科技结合,远程消融、导管自动到位等功能将逐步走进现实。

适当的消融损伤大小是射频消融成功的必要条件。
目前常用的消融系统中,通过压力、消融功率、导管稳定度、消融时间确定的消融指数(AI)或病灶大小指数(LSI)是反应消融深度的量化指标,对消融损伤有较高的指导意义。
在此基础上,高功率、低时程的消融策略能较好地提高消融效率。在AI指导下将消融功率提升到40W至50W,可以明确缩短消融时间,且不影响消融效果,同时消融时程缩短可以减少阻抗热对临近组织的损伤。
目前绝大部分的射频导管消融功率限制于50W,然而允许更高功率(上至90W)的射频导管(QDOT,强生医疗科技公司)已逐步在临床工作中应用,这将进一步提高房颤消融的效率及安全性。
房颤导管消融的基石是肺静脉隔离
除此之外存在诸多肺静脉外消融策略,例如左房线性消融、后壁隔离、左心耳隔离、碎裂电位消融、转子消融等。
虽然上述策略对房颤患者具有潜在获益,最新的国内外房颤指南及共识中仍未将上述肺静脉外消融作为常规术式推广。
在此背景下,射频导管通过点对点式的消融方式完成肺静脉隔离,其效率势必落后于各类针对肺静脉消融的球囊导管。曾经有数款射频球囊导管被开发及尝试应用于临床,但因各种原因上述导管并未被推广。不可否认,射频消融依然是最主流的消融能源,特别在需要结合高精密度标测以及心房内的局灶或线性消融的情况下,此时使用射频消融系统能潜在地提高消融手术的成功率。
“冷”-冷冻能量
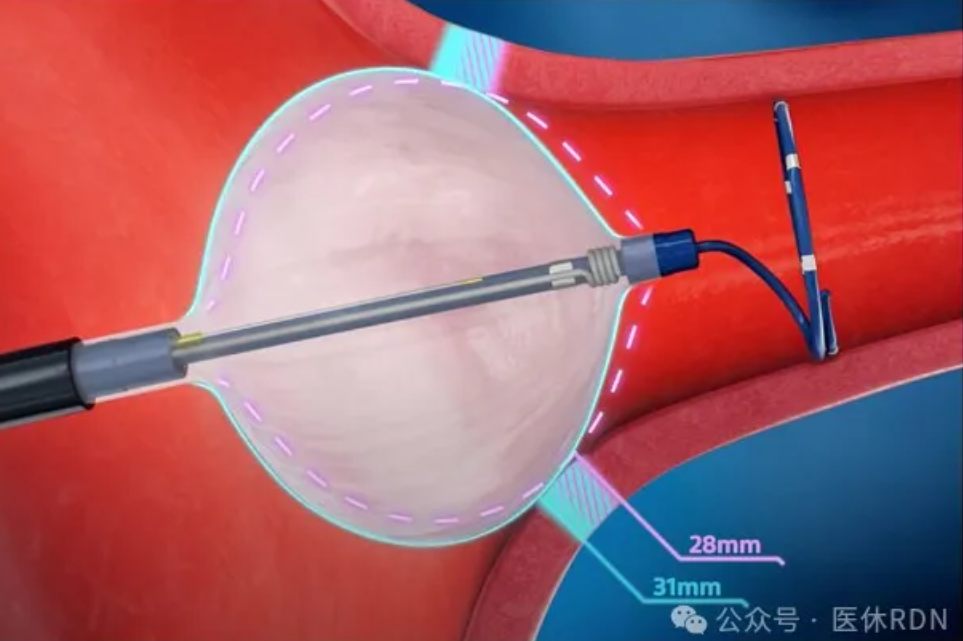
冷冻用于房颤消融晚于射频,2001年首先于欧洲获批,并于2013年进入中国。原理上,冷冻消融使用液态制冷剂,通常是“笑气”(N2O),当液态制冷剂通过极其细小的通道输送至球囊时,会经历Joule-Thomson效应,使与导管贴靠的组织温度降低,导致组织细胞内外形成冰晶,细胞脱水、蛋白质变性,最终导致局部组织的坏死。
尽管2016年发布的Fire and Ice研究结果提示冷冻与射频相比在有效性及安全性上无显著差异,在全因住院率、直流电复律率、心血管病因住院率、再消融率等多项二级终点上,冷冻仍然存在优势。
此外,冷冻还具有单次隔离率更高,损伤灶更为均质,血栓风险更低,学习曲线更短等优点。因此这项技术成为许多房颤新术者的优选。
自2013年至今,房颤冷冻消融已在国内跨越了10余年的发展历程,国内已有十多家中心累计应用病例数超过1000例,截至2017年已累计10000例。
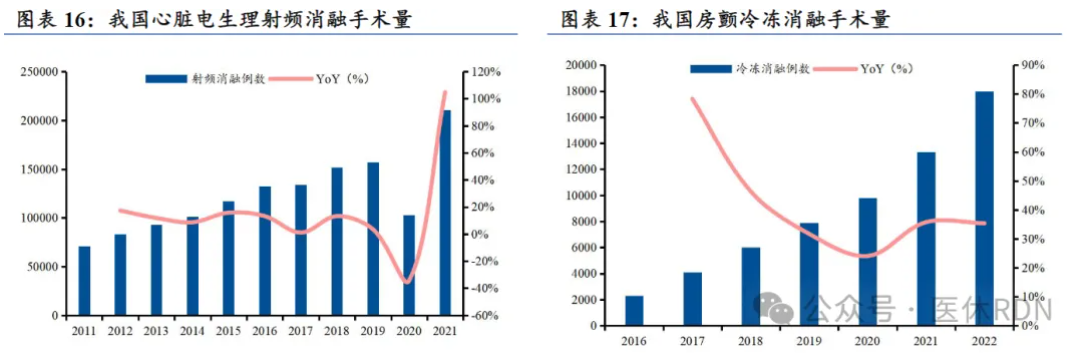
因此,为了规范冷冻球囊疗法,并普及这项技术,中华医学会心电生理和起搏分会联合中国医师协会心律学专业委员会于2020年发布了《经冷冻球囊导管消融心房颤动中国专家共识》。
房颤的进展和病残率及死亡率相关,荟萃研究发现,若不接受导管消融,阵发性房颤患者可有10%~20%的概率在一年内进展为持续性房颤。
EAST-AFNET4研究结果证实,早期节律控制可以降低包括心血管原因死亡、卒中、因心力衰竭加重或急性冠状动脉综合征而住院的复合终点。因此,尽早让初发房颤患者维持在窦性节律上,患者可获益更多。
那么,是首选导管消融还是药物控制呢?
三项将冷冻球囊消融作为阵发性房颤一线治疗的研究:STOP AF First,Early AF和Cryo First给出了明确的答案。与药物治疗相比,冷冻球囊导管消融治疗阵发性房颤初期患者疗效更佳,也相对安全。Progressive AF研究,作为Early AF延长随访至三年的观察性研究,发现冷冻消融组出现持续性房颤或复发性房性快速心律失常的发生率明显较低,冷冻消融组相较药物治疗能有效阻止阵发性房颤进展为持续性房颤。
常有术者对选择冷冻球囊消融存有顾虑,倘若患者确实存在肺静脉来源的触发灶,那冷冻消融效果是否确切。倘若患者肺静脉解剖变异,或是持续性房颤需要增加肺静脉隔离外的基质改良,冷冻球囊还能达到消融效果么?
有研究者发现,在血管内超声和三维系统的帮助下,冷冻球囊可安全有效地行肺静脉外基质改良。在这项研究中,所干预的肺静脉外基质包含左肺静脉与心耳交界的嵴部、左房顶部、左房后壁、上腔静脉、右心耳等部位。
随访一年时,阵发性房颤患者成功率为88%,持续性房颤患者为71%,长程持续性房颤患者为55%。KUNISS等则证明使用冷冻球囊行左房顶部线消融的可行性并探讨了消融技巧,证实可在88%患者中实现急性左房顶部线阻滞。
我们近期的研究发现,上腔静脉也可以安全地使用冷冻球囊隔离,只要确保球囊赤道面高于上腔静脉与右房连接处5mm以上,术中未出现窦房结损伤,且只有2.3%的患者出现一过性膈神经麻痹。
对于肺静脉存在解剖变异的情形,例如左肺静脉共干,球囊也可以有效的通过多种策略实现隔离。而对于更为特殊的下肺静脉共干,冷冻球囊消融则有效率更高的优势。
“光”-激光能量
激光能量是一种新型的消融能量,通过发射激光后,使组织吸收激光能量后产热而引起变性、坏死,已被应用于肿瘤、结石的治疗中。不同于射频、冷冻通过热能的增加或转移从而达到消融效果,激光消融基于光子的能量,通过体积热破坏组织;激光能量在内皮水平以下的心肌中达到了最大吸收,目前首选980nm激光进行心肌消融,平衡了激光的穿透性和损伤性,使得损伤集中于心肌中部,而基本不损失心内膜,从而降低了焦痂、血栓形成的风险。

激光消融系统由可调弯鞘、激光球囊、光纤内镜以及带有激光发生器的工作站所组成。激光球囊不同于其他的硬性球囊,具有高度顺应性,在封堵肺静脉时可通过球囊的形变,实现更良好的对接。
对于肺静脉变异的患者,激光球囊具有一定的优势。同时,激光球囊内径最高可充盈至38mm,其不仅可用于消融极端粗大的肺静脉,大尺寸的球囊可将消融范围扩大至肺静脉前庭,能够助力术者完成更多房颤基质的消融。
激光消融系统中配有光纤内镜,可用于直视球囊周围心脏解剖情况。相较于其他系统必须借助透视或是压力指数明确贴靠情况,内镜下直视球囊与心肌间位置关系能够更加直观反应贴靠。值得注意的是,内镜在导管轴上的偏心位置,内镜仅能显示300°的视野,因而必须通过旋转导管获得完全视野。希望未来在导管设计上能有所突破,扩大内镜可视范围,降低操作难度。
目前激光球囊是第三代产品,其最大更新点在于配备自动消融模式(Rapid模式)。不同于过去通过手动操作发射器手柄,使激光移动到定点位置进行消融,第三代球囊配备内置电机,带动激光发射器自动围绕杆身旋转,并进行连续消融,造成更加均匀、可靠的消融效果。研究报道,激光球囊的肺静脉单次消融隔离率高达92%,术后的有效性与安全性与射频消融及冷冻球囊消融相当。同时,自动消融模式下消融一根肺静脉的时间约为160s,极大程度提高肺静脉隔离的效率,有研究表明,使用第三代激光球囊的平均手术时间约104min。
激光消融系统未配备电极,需要额外电生理导管进行标测,我们希望新一代导管设计突破上述束缚。目前激光球囊处于国产化阶段,未来我们期待新一代国产球囊能够登陆房颤消融的舞台,能成为射频与冷冻之外的一股新力量。

“电”-脉冲电场能量
脉冲电场消融(PFA)的基本原理是电穿孔。细胞膜磷脂双分子层在电场作用下发生重排,形成纳米级亲水孔道,使细胞膜通透性增高,导致钾离子和酶的外泄,细胞内钙离子超载。最终细胞内稳态破坏,细胞走向凋亡或坏死。
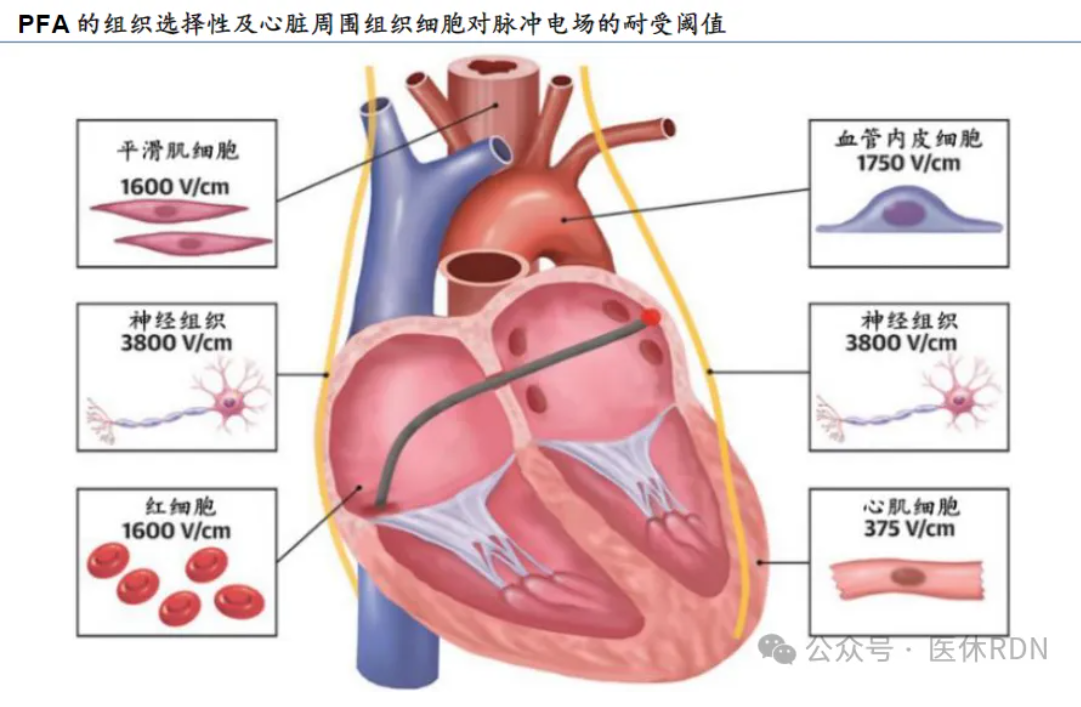
脉冲电场不仅可用于隔离肺静脉,同时也能用于局灶消融而实现线性隔离,或是区域性的成片消融,甚至消融以往热能消融存在安全隐患的心耳结构。
目前最大的PFA真实世界研究MANIFEST-PE研究共纳入1568名患者,报道的1年无房性心律失常率在阵发性房颤患者中是81.6%,持续性房颤患者中是71.5%,效果与传统能量比肩。ADVENT研究作为首个头对头比较PFA与传统热能消融(射频及冷冻)的随机对照研究,证实了PFA在阵发性房颤患者中,消融的安全性及成功率均不亚于射频及冷冻消融。KUEFFER等则比较了三种能量在持续性房颤患者中的效果,经混杂因素调整后,1年无房性心律失常的结果为:
冷冻球囊消融(CBA)组62.1%,PFA组55.3%,射频消融(RFA)组48.5%(CBA vs PFAP=0.79;CBA vs RFAP=0.79P=0.09;PFA vs RFA,P=0.010)。与射频消融相比,冷冻球囊消融和脉冲场消融在心律失常无复发生存方面的表现更佳。
若单独将PFA和冷冻球囊消融做比较,RUDOLPH等通过系统回顾11个涉及两种能量消融的研究,发现PFA在肺静脉隔离中相比冷冻球囊消融,能够缩短手术时间,降低心律失常复发率,并减少围手术期并发症。
拥有不逊于传统能量的成功率,广泛的应用场景,高效的消融效率,以及更为重要的心肌特异性损伤带来的安全性,PFA成为今后消融能源有力的竞争者。
在人体首次研究中,PFA显示出了极佳的安全性。严重的不良事件仅在0~2.5%的患者中发生。特别是没有热能相关的并发症发生,如热食管损伤或膈神经麻痹,也没有肺静脉狭窄的报道。对无症状患者进行的脑磁共振成像显示,无症状脑损伤的发生率在3%~19%之间变化,而既往射频消融发生率在6.8%~42%,冷冻消融发生率在5%~26.9%。
新技术既带来机遇也充满挑战。首先,虽然PFA避免了许多热能所致的并发症,但也带来了一些其他并发症。
其一,冠状动脉痉挛:PFA所致冠状动脉痉挛的发生与消融导管和血管之间的距离密切相关。
在二尖瓣及三尖瓣峡部消融时可导致冠状动脉痉挛,通过冠状动脉内应用硝酸甘油可缓解,也可以通过静脉药物应用预防。
其二,PFA术后可出现溶血及溶血诱导的肾功能衰竭。
一项回顾性研究报道,在17000余名使用花环状PFA导管治疗的房颤患者中,溶血诱导的肾功能衰竭发生率为0.03%。溶血的发生和消融的次数相关,70次消融是发生溶血的阈值,通过大量盐水灌注可避免其发生。若考虑在肺静脉隔离外增加基质改良,则需要特别注意这个并发症的发生。
其次,PFA对心脏自主神经系统的影响有别于其他能源,由于PFA的相对组织选择性,它可能不会永久性地影响心脏自主神经系统。与射频或冷冻能量相比,PFA消融后心脏迷走神经反应的减弱要少得多,并且这种反应很快恢复到基线。能源间不同的自主神经调控是否会对房颤或患者本就存在的心血管疾病远期预后产生影响尚不知晓,有待于将来的研究。
再次,PFA目前不推荐用于左房存在金属植入物的患者,例如存在左心耳封堵装置的患者,如何在这些人群中应用PFA便成为需要攻克的问题。采用PFA隔离上腔静脉已有报道,如何在有心脏电子植入物患者(例如起搏器植入患者)中使用PFA安全地隔离上腔也将成为一个将来论证的议题。
最后,国内参与设计和研发脉冲电场心脏消融的公司超过50余家,远多于射频和冷冻厂商。
我们对百花齐放,百家争鸣的局面既感欣喜,又有担忧。欣喜的是未来患者将有更多选择,民族品牌或有一席之地,忧虑的是PFA的效果不仅取决于导管形态,贴靠方式等外在因素,更取决于设置的电场场强,脉冲波参数等各个厂家受专利保护且无法公开的内在因素。这会使得术者难以直接比较各厂家的优劣,唯有尝试才能分高下。
本文2025-04-12 21:42:27发表“医休观点”栏目。
本文链接:https://www.yixiuqixie.com/article/713.html
阅读排行
- 新源脑科学完成数千万元Pre-A轮融资,加速脑功能监测与神经调控产品落地
- 加速注射笔产能布局,英捷信医疗顺利完成数千万元A轮融资
- 康复住院病案首页现存问题:主要诊断选择错误、遗漏、不规范、手术操作编码遗漏、入院病情与出院诊断不一致
- 健适医疗完成2500万美元战略融资,进一步增强企业产品研发能力和发展运营模式
- 靠大单品融资超13亿元,这家关节植入物制造商16年只做一个产品
- 拥有28家康复医院的明州医疗,面对医保违规问题也束手无策
- 基于运动想象范式,搭建独特算法,韶脑科技有望将脑卒中康复周期缩短1/3
- 射频消融+左心耳结扎术后患者死亡,医院被索赔27.5万元
- 收藏!RDN一般手术操作步骤
- 房颤消融:“冷-热-光-电”的交相辉映